En la ingeniería de tejidos de expansión celular 3d en biorreactores y la medicina regenerativa, el cultivo de condrocitos (las células responsables de mantener nuestro cartílago) presenta un reto único: estas células son dependientes de anclaje. En un matraz de cultivo tradicional, su crecimiento es limitado y bidimensional, lo que a menudo provoca que pierdan sus propiedades naturales.
Para superar estos límites, la biotecnología moderna combina dos herramientas poderosas: los microportadores y los biorreactores de movimiento ondulatorio (WAVE).
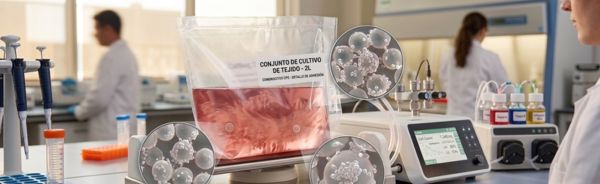
A diferencia de los sistemas de agitación mecánica convencionales que pueden dañar las membranas celulares mediante el esfuerzo de corte, el sistema WAVE 25 utiliza un balanceo suave y rítmico. Este movimiento genera una «ola» interna que mantiene los microportadores en suspensión, garantizando una oxigenación óptima y un entorno hidrodinámico de bajo impacto.
En este artículo, exploraremos el protocolo estandarizado para preparar este ecosistema dinámico, desde la rehidratación de los soportes hasta la estabilización de los parámetros críticos dentro del biorreactor.
Preparación de Microportadores y Cultivo de Condrocitos CP5 en Biorreactores
El uso de microportadores ha revolucionado el cultivo celular a gran escala, permitiendo que las células dependientes de anclaje, como los condrocitos, crezcan en sistemas de suspensión. En este artículo, desglosamos el protocolo esencial para la rehidratación de microportadores, la preparación del inóculo y el mantenimiento en un sistema de biorreactor.
1. Preparación y Esterilización de los Microportadores
El primer paso crítico es asegurar que los microportadores Cytodex 3 estén debidamente hidratados y estériles para recibir a las células.
- Rehidratación inicial: Pesar 300 mg de microportadores en un tubo Falcon de 50 mL y añadir 30 mL de DPBS (libre de
). Dejar incubar a temperatura ambiente durante 4 horas.
- Lavado: Tras la incubación, retirar el sobrenadante y realizar un lavado con 20 mL de DPBS fresco. Mezclar brevemente en vórtex.
- Esterilización: Sustituir el DPBS por 30 mL nuevos y someter a autoclave a 121°C con 1 bar de sobrepresión durante 25 minutos.
- Acondicionamiento: Una vez fríos, retirar el DPBS bajo campana de flujo laminar y añadir 30 mL de medio DMEM estéril. Incubar por 30 minutos para acondicionar la superficie de las esferas antes de transferirlas al contenedor final (Cellbag).
2. Preparación del Inóculo de Condrocitos CP5
Para garantizar un crecimiento óptimo, las células deben estar en su fase de mayor vitalidad.
- Control de Confluencia: Observar las células CP5 bajo el microscopio. El momento ideal para la transferencia es cuando alcanzan una confluencia de entre el 70% y el 90%.
- Tripsinización: Tras lavar las células con DPBS, añadir 3 mL de tripsina-EDTA. Una vez despegadas (aprox. 5 min), detener la reacción con 5 mL de medio DMEM.
- Concentración Celular: Centrifugar la suspensión a 3800 g por 5 minutos. Tras descartar el sobrenadante, resuspender en 5 mL de DMEM y ajustar la densidad celular a 6 x 105 células/mL.
3. Inoculación y Adhesión
Este es el momento donde las células se encuentran con su soporte físico.
- Transferir 30 mL de la dilución celular al Cellbag que contiene los microportadores acondicionados.
- Incubar el sistema a 37°C durante 4 horas. Este tiempo es vital para que los condrocitos se adhieran firmemente a la superficie externa de las microesferas.
- Finalizado este periodo, añadir 300 mL adicionales de medio DMEM para completar el volumen de trabajo.
4. Gestión del Biorreactor (Sistema WAVE 25)
Con las células ya adheridas, el sistema se traslada al biorreactor para su expansión celular controlada.
- Configuración: Instalar el Cellbag en el balancín del sistema WAVE 25 y estabilizar los parámetros ambientales.
- Condiciones Ideales: Mantener la temperatura a 37°C y la concentración de Oxígeno Disuelto (DO) al 100% de saturación (basado en una mezcla de gases de 21% O2, 5% CO2 y 74% N2).
- Monitoreo: Mantener el cultivo bajo agitación oscilatoria durante 7 días, realizando muestreos diarios de 5 mL para monitorear la salud y el metabolismo del cultivo.
Nota para investigadores: La precisión en los tiempos de incubación y la esterilidad del proceso son los factores que determinarán el éxito de la expansión celular de sus condrocitos.